随着2018年诺贝尔医学奖花落两位研究肿瘤免疫的免疫学家,以表彰他们“发现负性免疫调节治疗癌症的疗法方面的贡献”,让越来越多的肿瘤患者和家属对肿瘤免疫治疗更加熟悉。

2018年诺贝尔医学奖获奖者:James P.Allison和Tasuku Honjo
在2018诺贝尔医学奖获得者做出这些发现之前,肿瘤免疫治疗的临床研究进展缓慢。
而以PD-1和PD-L1抑制剂为代表的“免疫检查点疗法”使癌症治疗取得了革命性突破,从根本上改变了免疫治疗在癌症治疗中地位。
在免疫检查点疗法越来越普及的同时,无论是肿瘤医生还是肿瘤患者,也面临着更多的问题。
如何更好地应用肿瘤免疫治疗为患者带来更多生存获益,减少免疫治疗的不良反应,成为当下亟待解决的热点。
免疫治疗的生物标志物
疗效预测的试金石
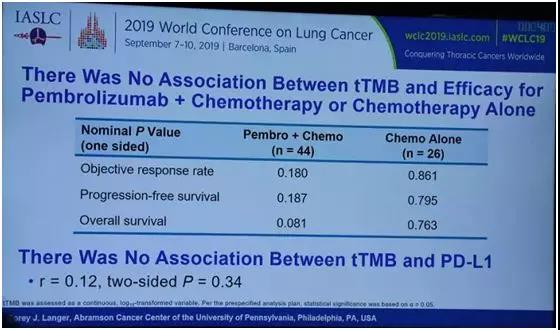
在刚刚结束的世界肺癌大会上,一项肿瘤组织突变负荷(tTMB)是否能预测帕博利珠单抗(K药)疗效的相关研究引起了大家的热议。
该项研究结果表明,肿瘤突变负荷与帕博利珠单抗联合化疗或者安慰剂联合化疗一线治疗转移性非鳞状非小细胞肺癌的疗效没有显著相关性。
帕博利珠单抗联合化疗在高肿瘤突变负荷和低肿瘤突变负荷的患者中有相似的生存获益。
因此,研究者认为肿瘤突变负荷在帕博利珠单抗联合化疗一线治疗转移性非鳞非小细胞肺癌的临床应用中可能有限。
这个阴性的研究结果让大家进一步意识到,临床上如何通过不同生物标志物筛选出能从免疫治疗中获益的患者仍然存在很多疑问。
但从已有的研究来看,已有部分生物标志物可以很好的预测免疫治疗的疗效。
1.PD-L1
首先是肿瘤组织中PD-L1表达的预测作用,前期有一项收录了20项临床研究的分析发现,PD-L1是否表达与肺癌、泌尿系统肿瘤和黑色素瘤的免疫治疗疗效相关,PD-L1表达患者的有效率比不表达患者的有效率高近一倍,并且PD-L1表达程度越高,免疫治疗疗效越佳。
以纳武单抗(O药)为例,以PD-L1表达是否大于10%为界限,可以明显区分出其在非鳞非小细胞肺癌中的治疗差异。
同样,在帕博利珠单抗治疗非小细胞肺癌的研究中,也发现PD-L1表达与患者治疗预后休戚相关,虽然对PD-L1表达的患者免疫治疗均有效,但PD-L1表达大于50%的患者疗效更佳。
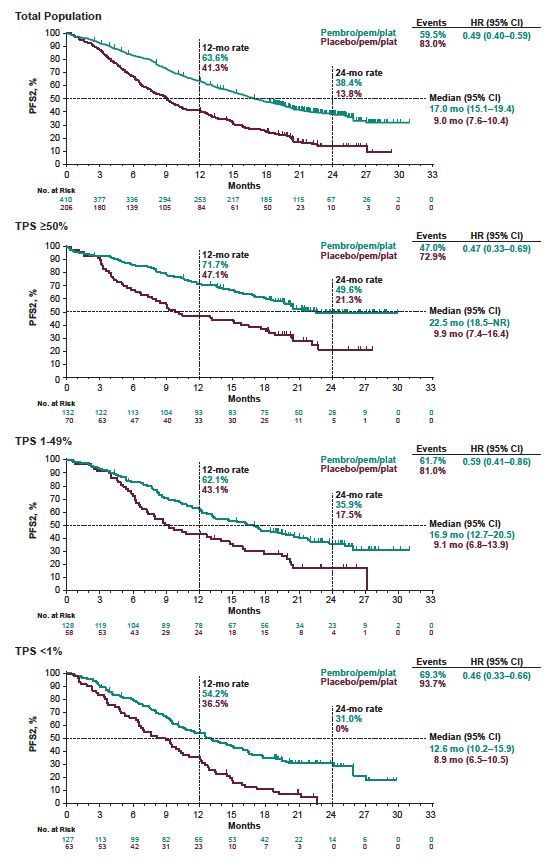
KEYNOTE-189研究(2019ASCO大会)
类似的,PD-L1单抗达武单抗的相关研究也得出了类似的结果。
但值得注意的是,目前不同研究在PD-L1检测中使用的检测抗体并不相同,因此,在解读PD-L1表达的结果时需要分别对待。
并且,随着治疗模式的改变,化疗与免疫治疗药物的结合也可以让更多PD-L1表达有限的患者明显获益。
2.肿瘤组织突变负荷
其次是肿瘤组织突变负荷(tTMB),虽然在今年的世界肺癌大会上,肿瘤突变负荷被认为并不能很好地预测K药在转移性非鳞非小细胞肺癌的疗效,但在长期的研究历程中,TMB还是被认为是与PD-L1表达相独立的一个很好的预测因子。
从机理上来说,患者TMB突变总负荷大,产生的新抗原多,肿瘤会被大量肿瘤特异性T细胞攻击,抗PD-1治疗可以使肿瘤T细胞反应得以更充分的发挥,因此更高突变负荷肿瘤对抗PD-1更敏感。
在多项研究中也发现,针对泌尿系统肿瘤,肺癌,乳腺癌,头颈部肿瘤等多个瘤种的预测中,位于前10%肿瘤突变负荷的患者疗效最佳。
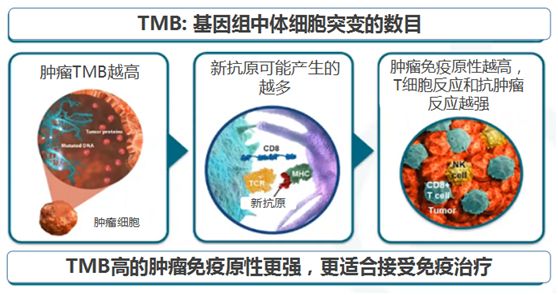
以非小细胞肺癌为例,TMB就因为被认可用来预测O药的疗效而写进的多个治疗指南。
但一直存在两个问题困扰了TMB作为预测因子的应用:
一是临界值问题,究竟怎样的TMB临界值可以区分有效或者无效患者尚存在疑问;
二是不同的检测机构因检测的突变基因库不同而存在差异,如何实现统一尚待后续验证。
3.错配修复基因缺陷
再次就是错配修复基因缺陷(dMMR)在大肠癌、胃癌以及消化系统肿瘤中也显示出上佳的预测作用,特别是在肠癌中,目前dMMR患者接受免疫治疗的疗效已获得了明确的结论。
另外,诸如POLE基因突变,胃癌中EBV阳性型等少见的预测因子也可以应用在免疫治疗的预测中。
也有部分研究认为,除了正向预测因子,也存在负向预测免疫治疗疗效不佳的因子甚至能够预测患者是否会因接受免疫治疗出现超进展的因子,但这些研究尚无明确定论,需更多的研究数据支持。
免疫治疗的疗效评价
假进展还是真进展
免疫治疗的疗效评价也是免疫治疗给肿瘤治疗带来的新课题。
在传统治疗中,肿瘤的疗效评价通常通过影像学评估就能得出明确的结论,肿瘤缩小意味着疗效较好,反之则意味着疗效欠佳。
而在免疫治疗中,却存在假性进展的现象。
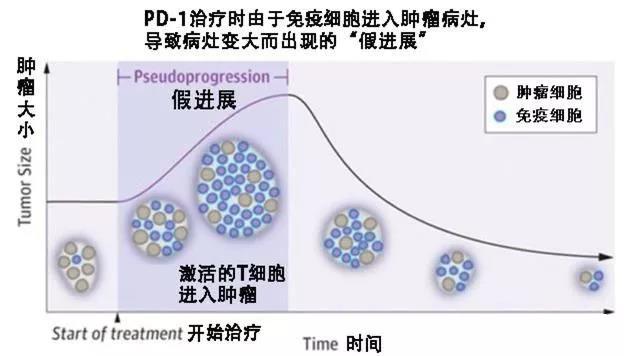
由于免疫治疗早期大量免疫细胞的局部浸润,让肿瘤看起来似乎增大了,但治疗实际却是明确有效的。
以非小细胞肺癌脑转移为例,一项回顾性研究发现约有5%左右的患者都属于这种假性进展。
因此,目前认为,传统的评价标准可能并不适用于免疫治疗的疗效评估,综合结合患者一般情况,症状改善情况,影像学评估等因素的免疫评价标准更适合于免疫治疗。
免疫治疗的不良反应
轻微还是致命?
由于不良反应机制不同,免疫治疗的不良反应与传统治疗大相径庭,大多数免疫相关不良反应为轻到中度,因此,大部分患者在接受免疫治疗后不会感到诸如恶心呕吐、脱发、乏力等化疗常见的不良反应。
在前期的研究中也发现,无论是总的不良反应发生率还是严重不良反应的发生率,免疫治疗均要低于化疗。
但对1-2%的少数患者来说,严重或危及生命的免疫治疗不良反应也有发生, 严重时可能导致患者死亡。
免疫治疗不良反应(irAE)的常见于皮肤、胃肠道、肝、肺、内分泌器官,而心脏、肾脏、神经、眼等相对少见。
针对既往存在间质性肺炎或者自身免疫性疾病等基础疾病的患者,由于免疫治疗带来致命性不良反应的可能性更大,因此,使用前需要更加慎重。
大部分不良反应在接受治疗后的1-6个月内发生,目前治疗上更多采取停药或者激素治疗的模式进行,通过治疗大多数治疗反应可以逆转。
因此,总体评估,免疫治疗的毒性还是会低于传统治疗。针对偶发的严重反应,随着治疗的普及和深入,也不再成为致命的治疗风险。

总的来说,免疫治疗具有持久的治疗活性,对于部分患者显示出治愈潜能,是目前和未来的治疗趋势。
但如何通过标志物寻找获益人群,通过合适的评价方式对获益进行准确评价,并在治疗中有效控制不良反应,仍是未来免疫治疗的热点和难点。
作者:陈佳琪主治医师
常常去帮助,总是在安慰。康复之路易加医与您同行。如果您觉得这篇文章对您有帮助,欢迎关注易加医官网或下载易加医APP。易加医是专注于肿瘤领域的互联网医疗服务平台,为肿瘤患者和家属提供肿瘤预防、就医、诊疗、康复所需的各类服务。



 浙公网安备 33010602004553号
浙公网安备 33010602004553号


