3月28日,EGFR和ALK阴性的转移性非鳞状非小细胞肺癌(NSCLC)患者又赢来一则好消息!一线治疗非鳞状NSCLC疗法Keytruda新适应症上市申请已经在国内获批!
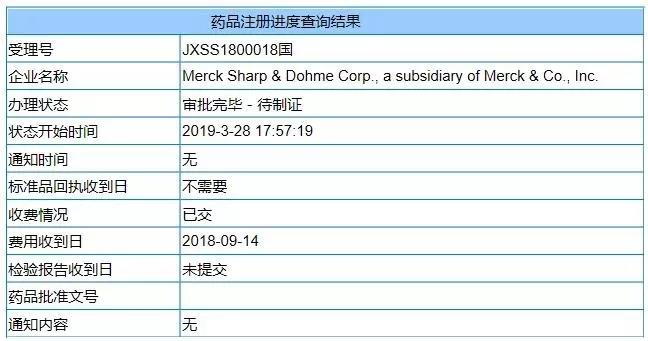
在国家药品监督管理局(http://samr.cfda.gov.cn/WS01/CL0025/) 网站上最新的药品注册进度查询结果显示,Keytruda新适应症的上市申请(JXSS1800018)已经通过,联合培美曲塞、顺铂一线治疗EGFR和ALK阴性的转移性非鳞状非小细胞肺癌(NSCLC)。
这一项审批通过主要是基于III期临床研究KEYNOTE-189公布的研究结果。该研究显示对于既往未接受过任何全身治疗的转移性非鳞NSCLC患者,帕博利珠单抗(pembrolizumab,Keytruda)联合化疗组的无进展生存期和总生存期较单用化疗组显著延长。
经过10.5个月的中位随访,可以观察到与对照组相比,K药联合培美曲塞与铂类化疗治疗转移性非鳞NSCLC患者死亡风险降低51%(HR=0.49),其中PD-L1>50%高表达组患者死亡率降低58%(HR=0.42)。
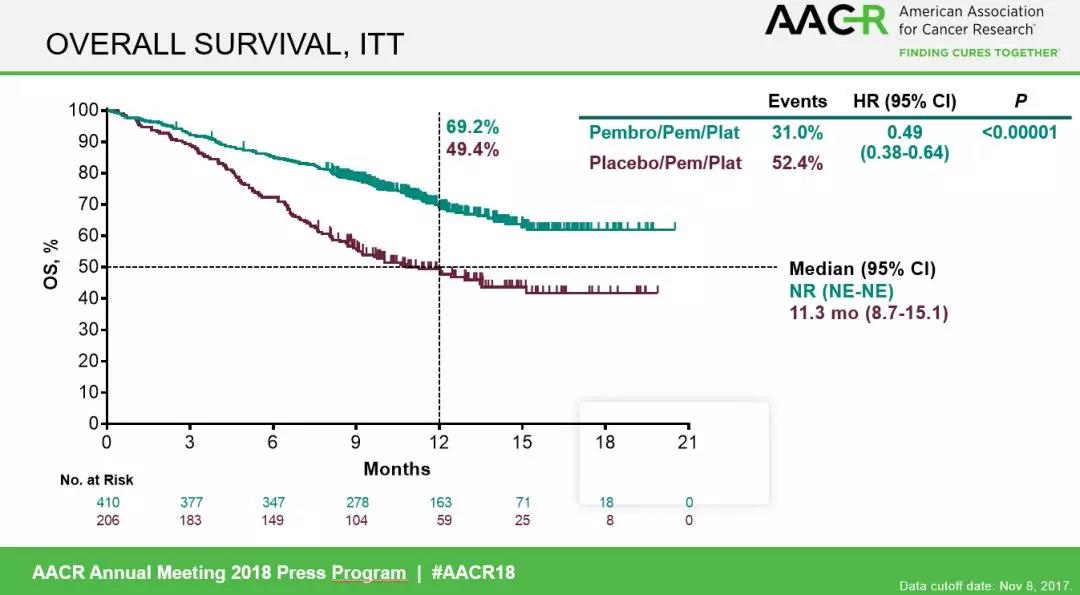
▲上图来自AACR会议KEYNOTE-189研究结果的汇报PPT
Keytruda+培美曲赛+卡铂方案于2017年首次获FDA(美国食品和药物管理局)批准一线治疗转移性非鳞状NSCLC。
2018年8月,又获得FDA的扩展标签审批,联合Alimta(pemetrexed,培美曲赛)及铂类化疗,用于无EGFR或ALK基因组肿瘤畸变的NSCLC患者的一线治疗。
在中国市场,Keytruda于2018年7月25日获批,成为继百时美施贵宝Opdivo之后第2个正式在中国上市的PD-1/PD-L1单抗类药物。
值得一提的是,Keytruda是首个同时获批作为联合用药和单药一线治疗转移性NSCLC的PD-1免疫疗法。
Keytruda发威!非小细胞肺癌治疗可首选免疫疗法!
无论从发病率还是致死率看,肺癌都是当之无愧的“癌王”。其中,非小细胞肺癌(NSCLC)是最常见的一类,约占肺癌的80-85%,包括鳞癌、腺癌、大细胞癌等。
非小细胞肺癌早期症状不明显,多数患者确诊时已出现进展或转移。不过,近年来,随着PD-1/PD-L1等免疫疗法的问世,晚期非小细胞肺癌的治疗已今非昔比。2017年美国临床肿瘤协会(ASCO)在《临床肿瘤学杂志》(JCO)发布的IV期非小细胞肺癌的临床实践指南中,就加入了免疫疗法的内容。
而在PD-1抑制剂临床应用中,目前主要是Opdivo(简称O药)和Keytruda(简称K药)。
Keytruda(中文商品名:可瑞达;通用名:帕博利珠单抗,pembrolizumab)是肿瘤免疫治疗巨头默沙东(Merck & Co)抗击NSCLC的重要武器。在美国国立卫生研究院 National Institutes of Health的网站上是这样介绍的:

用于治疗黑色素瘤(一种皮肤癌),手术治疗不成功,并已扩散到身体其他部位;
用于单独或与其他化疗药物联合治疗已扩散到邻近组织或身体其他部位的某些类型的非小细胞肺癌(NSCLC)
自2014年Opdivo和Keytruda先后获美国FDA批准上市以来,两个PD-1药物之间的较量从未停止过。但是在肺癌领域,K药的临床试验数据呈现霸主地位。特别是在NSCLC的免疫治疗领域,临床数据显示Keytruda已经占据绝对领导地位。
我们可以来一起回顾一下既往的临床结果:
01:在关键性III期临床研究KEYNOTE-042中,Keytruda单药一线治疗非小细胞肺癌(NSCLC)显著延长了总生存期(OS),达到了研究的主要终点。
研究结果显示,由DMC开展的一项中期分析表明,与含铂化疗(卡铂+紫杉醇或卡铂+培美曲赛)相比,Keytruda单药治疗在PD-L1 TPS≥1%的患者中显著延长了OS。作为预先指定分析计划的一部分,DMC依次对TPS≥50%、≥20%、≥1%的患者进行了评估,结果显示,Keytruda在TPS≥50%、TPS≥20%以及整个研究人群(TPS≥1%)中均显著延长了OS。该研究中,Keytruda的安全性与之前报道的Keytruda单药治疗晚期NSCLC的研究中一致。
02:默沙东和礼来联合开展的关键性III期临床研究KEYNOTE-189的数据显示,联合Alimta及含铂化疗一线治疗NSCLC的可以显著改善OS和PFS。
数据显示,与单纯化疗组相比,Keytruda治疗组OS实现了统计学意义和临床意义的显著改善(中位OS:未达到 vs 11.3个月,HR=0.49[95%CI:0.38-0.64],p<0.00001)、死亡风险降低一半。此外,与单纯化疗组相比,Keytruda治疗组PFS也实现了显著改善(中位PFS:8.8个月 vs 4.9个月,HR=0.52[95%CI:0.43-0.64],p<0.00001)。次要终点方面,Keytruda治疗组ORR显著提高(48% vs 19%,p<0.00001)、DOR实现延长(11.2个月 vs 7.8个月)。
应该感谢这些研究机构和专家,始终不懈地致力于改善患者生存结果,为更多的肺癌患者带来了希望!让我们共同期待Keytruda带来更多的好消息吧!
文章参考来源:
1、FDA Approves Expanded Label for Merck’s KEYTRUDA® (pembrolizumab) in Combination with Pemetrexed (ALIMTA®) and Platinum Chemotherapy for First-Line Treatment of Patients with Metastatic Nonsquamous NSCLC, with No EGFR or ALK Genomic Tumor Aberrations
2、Merck’s Keytruda Nabs Another Approval, This One Under FDA’s Real-Time Program
3、https://medlineplus.gov/druginfo/meds/a614048.html
4、http://ascopubs.org/doi/full/10.1200/JCO.2017.74.606
5、https://www.businesswire.com/news/home/20181030006098/en/FDA-Approves-Merck%E2%80%99s-KEYTRUDA%C2%AE-pembrolizumab-Combination-Carboplatin
常常去帮助,总是在安慰。康复之路易加医与您同行。如果您觉得这篇文章对您有帮助,欢迎关注易加医官网或下载易加医APP。易加医是专注于肿瘤领域的互联网医疗服务平台,为肿瘤患者和家属提供肿瘤预防、就医、诊疗、康复所需的各类服务。
易加医 2019.3.29



 浙公网安备 33010602004553号
浙公网安备 33010602004553号


