乳腺癌是女性常见的恶性肿瘤,其中HER-2表达阳性者约占20-30%。HER-2阳性的乳腺癌,具有浸润性强、进展快速、复发风险高和预后差等临床特点。

近年来,随着曲妥珠单抗等抗HER-2治疗靶向药物的不断出现,HER-2阳性乳腺癌患者的预后得到较大幅度的提高。今天,我们就来盘点一下近年来上市、研发的用于HER-2阳性乳腺癌患者的新药。
01:曲妥珠单抗
HER-2一线治疗首选
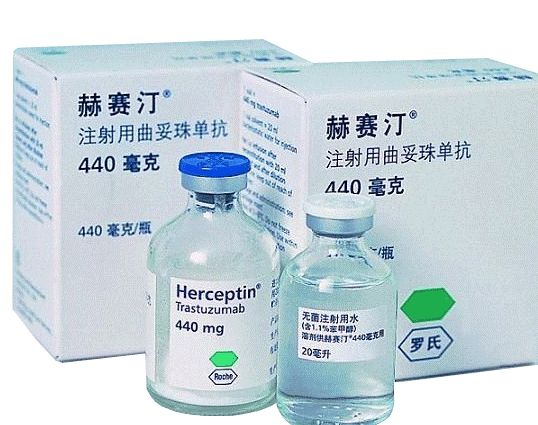
通用名:曲妥珠单抗(Trastuzumab)
商品名:赫赛汀(Herceptin)
生产商:罗氏制药
靶点:HER-2
中国是否上市:已上市,已纳入国家医保目录
中国已获批乳腺癌适应症类型:新辅助,辅助,晚期或转移性一线、二线及后线
作为第一个获批上市的HER-2单克隆抗体药物,曲妥珠单抗具有划时代的意义,开创了乳腺癌分子靶向治疗的新纪元。该药最初于1998年在美国批准上市。
2002年在中国获批上市。目前获批的适应症为:作为单一药物治疗已接受过1个或多个化疗方案的HER-2过度表达的转移性乳腺癌;与紫杉类药物合用治疗未接受过化疗的HER-2过度表达的转移性乳腺癌;单药适用于接受了手术、含蒽环类抗生素辅助化疗和放疗(如果适用)后的HER-2过度表达乳腺癌的辅助治疗;与化疗联合新辅助治疗,继以辅助治疗,用于局部晚期(包括炎性)或者肿瘤直径>2cm的乳腺癌。
超过70%的早期乳腺癌患者使用赫赛汀后获治愈;赫赛汀联合标准化疗,还能显著提高转移癌患者的无病生存率,创造了转移性乳腺癌治疗上的空前生存优势。
正是基于在乳腺癌治疗中的突出表现,赫赛汀因此被很多乳腺癌患者称为“救命药”。自从1998年美国上市以来,全球已经有超过100万的HER-2阳性乳腺癌患者,从使用曲妥珠单抗中获益。
02:帕妥珠单抗
妥妥方案疗效惊人
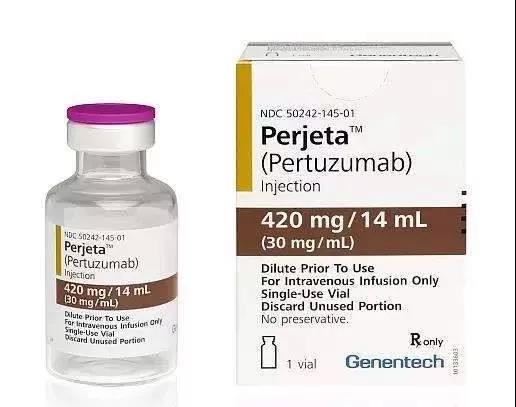
通用名:帕妥珠单抗(Pertuzumab)
商品名:帕捷特(Perjeta)
生产商:罗氏制药
靶点:HER-2
中国是否上市:已上市,已纳入国家医保目录
中国已获批乳腺癌适应症类型:新辅助,辅助,晚期或转移性一线(与曲妥珠单抗联合使用)
帕妥珠单抗是重组人源化HER-2单克隆抗体,最初为2012年6月8日在美国获批上市。
2018年12月17日获中国国家药品监督管理局批准上市,当时适应症为:与曲妥珠单抗和化疗联合,用于HER-2阳性、局部晚期、炎性或早期乳腺癌患者(直径>2cm或淋巴结阳性)的新辅助治疗,作为早期乳腺癌整体治疗方案的一部分;也可用于具有高复发风险的HER-2阳性早期乳腺癌患者的辅助治疗。
2019年12月10日,罗氏制药中国宣布,中国国家药品监督管理局正式批准了帕妥珠单抗联合曲妥珠单抗和多西他赛,联用于尚未接受抗HER2治疗或化疗的HER2阳性转移性乳腺癌患者的一线标准治疗方案。
妥妥双靶(曲妥珠单抗+帕妥珠单抗)改写了HER-2阳性晚期乳腺癌治疗结局,将患者中位生存期提升到57.1个月,提高了16.3个月,且37%患者达到八年生存,显著高于曲妥珠单抗+化疗组的23%。
03:T-DM1
解决曲妥珠单抗耐药困局

通用名:恩美曲妥珠单抗(Trastuzumab Emtansine,T-DM1)
商品名:赫赛莱(Kadcyla)
生产商:罗氏制药
靶点:HER-2
中国是否上市:已获批,未上市
中国已获批乳腺癌适应症类型:辅助(曲妥珠单抗治疗失败后)
T-DM1是全球首个应用于实体瘤的抗体药物偶联剂(antibody-drug conjugate,ADC),由抗HER-2单克隆抗体曲妥珠单抗和细胞毒药物DM1(美登素衍生物)通过连接子偶联而成,具有靶向性和细胞毒杀伤双重抗肿瘤作用。
2013年2月获美国FDA批准,T-DM1用于治疗已经接受过曲妥珠单抗和一线紫杉烷类化疗无效的HER-2阳性晚期乳腺癌患者。2019年5月6日,美国FDA又批准T-DM1用于紫杉烷+曲妥珠单抗新辅助治疗后存在残存病灶的HER-2阳性早期乳腺癌患者的辅助治疗。
2020年1月22日,罗氏制药中国宣布,国家药品监督管理总局正式批准创新靶向药物赫赛莱,单药适用于接受了紫杉烷类联合曲妥珠单抗为基础的新辅助治疗后仍残存侵袭性病灶的HER-2阳性早期乳腺癌患者的辅助治疗。
疗效方面,辅助治疗,HER-2阳性早期乳腺癌新辅助治疗完成后有残存病灶的患者,辅助治疗使用T-DM1可相较于曲妥珠单抗,使乳腺癌复发风险降低50%;二线及后线治疗方面,T-DM1治疗数据为中位无进展生存期9.6个月,中位总生存期30.9个月,客观缓解率43.6%,中位缓解持续时间12.6个月。
T-DM1的应用,让曲妥珠单抗治疗失败的患者,依然可以通过抗HER-2治疗获得良好生存获益。
04:拉帕替尼
第二个上市的乳腺癌分子靶向药物,为曲妥珠单抗治疗失败患者带来希望
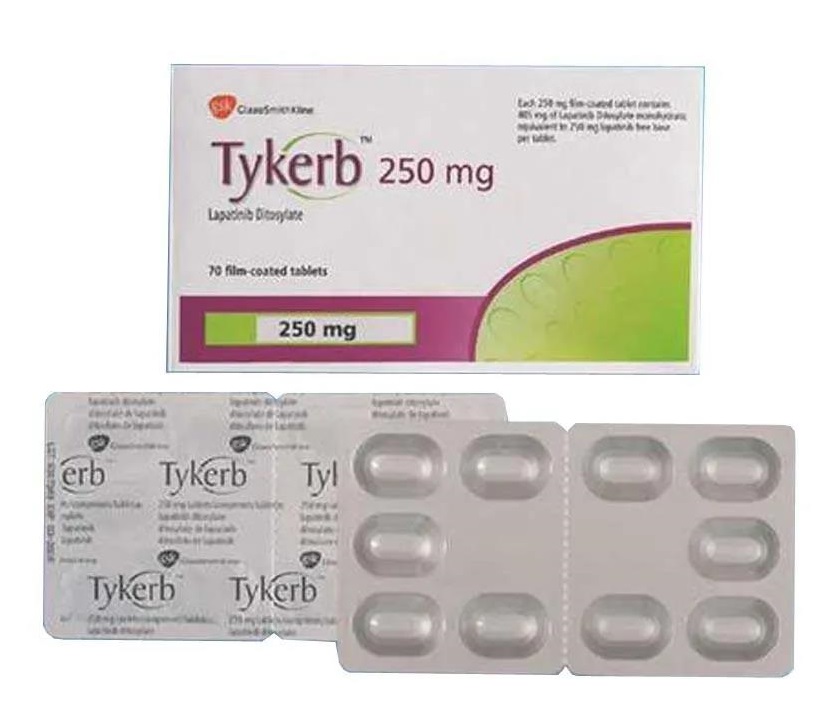
通用名:拉帕替尼(Lapatinib)
商品名:泰立沙(Tykerb)
生产商:诺华制药/葛兰素史克制药
靶点:HER-1(EGFR)/HER-2
中国是否上市:已上市
中国已获批乳腺癌适应症类型:晚期或转移性一线、二线及后线(曲妥珠单抗治疗失败后)
拉帕替尼是一种口服的小分子表皮生长因子酪氨酸激酶抑制剂,能有效抑制人类表皮生长因子受体-1(ErbB1,HER-1,EGFR)和人类表皮生长因子受体-2(ErbB2,HER-2)酪氨酸激酶活性,通过多种途径发挥作用,抑制或杀死肿瘤细胞。拉帕替尼是继曲妥珠单抗之后第二个上市的乳腺癌分子靶向药物,最初于2007年在美国获批上市。
2007年3月14日,美国食品药品管理局批准拉帕替尼和卡培他滨联用治疗人表皮因子受体2(ErbB2,HER-2)过度表达且经蒽环类药物、紫杉醇和曲妥珠单抗治疗过的晚期或者转移性乳腺癌患者。2010年FDA又批准拉帕替尼联合芳香酶抑制剂来曲唑治疗曾接受激素治疗并且 HER-2阳性、激素受体(HR)阳性的转移性乳腺癌患者。
2013年,拉帕替尼于中国上市,可用于治疗HER-2阳性且既往接受过包括蒽环类、紫杉类、曲妥珠单抗治疗的晚期或转移性乳腺癌患者。
研究结果显示,拉帕替尼联合卡培他滨,中位疾病进展时间:27.1周;缓解率:23.7%;中位总生存期:75周。
拉帕替尼联合卡培他滨的方案,成为曲妥珠单抗治疗失败的晚期乳腺癌患者的可选方案。但拉帕替尼的地位受到了更多药物的挑战。
05:吡咯替尼
首个中国研发的HER-2药物,挑战拉帕替尼地位

通用名:吡咯替尼(Pyrotinib)
商品名:艾瑞妮(Airuini)
生产商:恒瑞医药
靶点:HER-1/HER-2
中国是否上市:已上市,已纳入国家医保目录
中国已获批乳腺癌适应症类型:晚期或转移性一线、二线及后线
吡咯替尼是不可逆的小分子受体酪氨酸激酶抑制剂,可显著抑制EGFR(HER-1)和HER-2,是由国内知名肿瘤药企恒瑞制药自主研发的1.1类新药,可谓填补了国内自主研发抗HER-2药物的空白。
2018年8月13日通过优先审评审批程序获准在中国上市,适应症为联合卡培他滨,用于治疗HER-2阳性、既往未接受或接受过曲妥珠单抗的复发或转移性乳腺癌患者,且先前患者接受过蒽环类和紫杉类化疗。临床研究显示吡咯替尼在一二线治疗均由良好疗效。
研究结果显示,既往接受过紫杉烷和曲妥珠单抗治疗的HER-2阳性乳腺癌患者,给予吡咯替尼+卡培他滨方案,PFS可达11.1个月,ORR达到68.6%。这一结果,直接挑战了拉帕替尼在曲妥珠单抗治疗失败后的地位。
06:来那替尼
抗HER-2三线治疗及脑转移患者的希望

通用名:来那替尼(奈拉替尼,Neratinib)
商品名:Nerlynx
生产商:彪马生物
靶点:HER-1/HER-2/HER-4
中国是否上市:未获批,未上市
美国获批乳腺癌适应症类型:辅助维持(曲妥珠单抗治疗后),晚期及转移性三线及后线(可用于多种抗HER-2药物治疗失败后)
来那替尼是一种口服的、不可逆的酪氨酸激酶抑制剂。
2017年7月,美国FDA批准来那替尼用于HER-2阳性早期乳腺癌患者手术后使用曲妥珠单抗后的维持治疗。在ExteNET试验中,对于早期HER-2阳性乳腺癌患者,用来那替尼维持治疗,患者的两年无病生存率可达到94.2%。
除去维持治疗,来那替尼广泛的靶点覆盖和特殊的HER-2胞内的ATP结合蛋白区,可以很好的抑制导致曲妥珠单抗耐药的旁路激活,从而逆转耐药。因此对于胞外HER-2靶药曲妥珠单抗、帕妥珠单抗、拉帕替尼及T-DM1耐药后可以考虑来那替尼为主的方案治疗。
临床研究结果显示,来那替尼的三线以后的治疗数据及脑转移治疗数据更为后线增加武器。按患者是否使用过拉帕替尼,分为拉帕替尼未治疗组(3A组)及拉帕替尼治疗组(3B组)。在3A组中,脑转移灶的ORR = 49%, 3B组脑转移灶的ORR = 33%。3A组和3B组中位PFS分别为5.5个月和3.1个月,中位OS分别为13.3个月和15.1个月。而头对头的NALA研究中,来那替尼+卡培他滨和拉帕替尼+卡培他滨的6个月PFS率分别为47.2%和37.8%,12个月PFS率分别为28.8%和14.8%。来那替尼无论在未使用或使用过拉帕替尼的患者中,都显示出较好疗效。
07:DS-8201
点燃抗HER-2多线治疗失败后患者,长期生存的希望
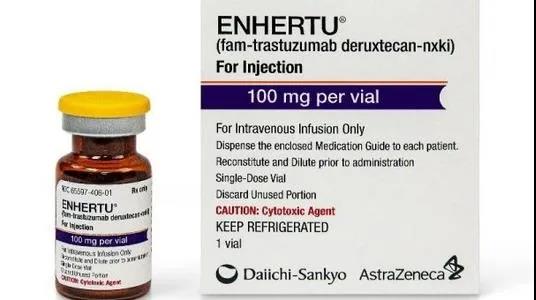
通用名:Trastuzumab Deruxtecan(DS-8201)
商品名:Enhertu
生产商:阿斯利康/第一三共
靶点:HER-2
中国是否上市:未获批,未上市
美国获批乳腺癌适应症类型:晚期及转移性三线及后线(2种及以上抗HER-2药物失败后)
DS-8201与T-DM1类似,是新一代ADC药物,通过一种4肽链接子,将靶向HER-2的人源化单克隆抗体曲妥珠单抗与一种新型拓扑异构酶1抑制剂exatecan衍生物(DX-8951衍生物,DXd)链接在一起,可靶向递送细胞毒药物至肿瘤细胞内,与通常的化疗相比,可减少细胞毒药物的全身暴露,从而减少毒副作用。
在美国,Enhertu于2019年12月获得加速批准,用于在转移性疾病中已接受过2种或2种以上抗HER-2药物治疗的HER-2阳性转移性乳腺癌成人患者。
2020年3月28日,日本厚生劳动省(MHLW)已批准Enhertu(DS-8201),用于治疗HER-2阳性、不可切除性或转移性、在先前化疗后复发的乳腺癌患者(限用于对标准治疗无效或不耐受的患者)。
DESTINY-Breast01临床试验显示,在先前接受过T-DM1治疗的HER-2阳性不可切除和/或转移性乳腺癌患者中,DS-8201的客观缓解率(ORR)为60.9%,包括11例患者肿瘤完全消失,疾病控制率为97.3%,临床获益率为76.1%,中位缓解持续时间(DoR)为14.8个月,中位无进展生存期(PFS)为16.4个月。试验尚未达到患者中位总生存期(OS),患者1年生存率估计为86%。
该研究最大的亮点在于,一半以上的受试者接受过6种药物治疗,包括以赫赛汀为代表的靶向药和内分泌药物,属于重度难治的乳腺癌患者。HER-2阳性乳腺癌患者在用尽几乎所有药物治疗后,再采取DS-8201治疗依旧能够获得60.9%的客观缓解率,数据可谓惊人。
综上所述,HER-2阳性的乳腺癌患者,有多种药物可选择。
抗HER-2药物中国已获批适应症定位
新辅助治疗:赫赛汀、帕捷特
辅助治疗:赫赛汀、帕捷特、赫赛莱
辅助维持:Nerlynx(赫赛汀辅助治疗后)
一线治疗:赫赛汀、帕捷特、泰立沙(赫赛汀失败后)、艾瑞妮
二线治疗:赫赛汀、泰立沙(赫赛汀失败后)、艾瑞妮
三线及后线治疗:赫赛汀、泰立沙(赫赛汀失败后)、艾瑞妮、Nerlynx(多种抗HER-2药物治疗失败后)、Enhertu(2种及以上抗HER-2药物失败后)
我们有理由坚信,未来会有更多的新药层出不穷,为HER-2阳性的乳腺癌患者带来更多生的希望,让患者不再感受到绝望。
常常去帮助,总是在安慰。康复之路易加医与您同行。如果您觉得这篇文章对您有帮助,欢迎关注易加医官网或下载易加医APP。易加医是专注于肿瘤领域的互联网医疗平台,为肿瘤患者和家属提供肿瘤预防、就医、诊疗、康复所需的各类服务。



 浙公网安备 33010602004553号
浙公网安备 33010602004553号


