3月8日,美国食品和药物管理局(FDA)优先通过了罗氏(Roche)集团下的阿特珠单抗(Atezolizumab)联合化疗一线治疗无法切除的局部晚期或转移性PD-L1阳性的三阴性乳腺癌(TNBC)的评审。这意味着Atezolizumab成为首个被批准用于乳腺癌的免疫疗法。
Atezolizumab属于PD-L1肿瘤免疫疗法之一,是当前备受瞩目的一类肿瘤免疫疗法。旨在利用人体自身的免疫系统抵御癌症,通过阻断PD-1/PD-L1信号通路使癌细胞死亡。
该组合基于IMpassion130试验,是首个在三阴性乳腺癌治疗中,显示出积极成果的3期免疫疗法研究。
Atezolizumab显著降低了疾病进展或死亡的风险,在意向治疗(ITT)人群中,与安慰剂相比,atezolizumab显着降低了疾病进展或死亡的风险(无进展生存期; PFS)(中位PFS = 7.2对5.5个月;风险比[HR] = 0.80 ,95%置信区间[CI],0.69-0.92,P = .0025)。
Atezolizumab也改善了中位总生存期(OS),但在中期分析时未达到统计学显著性差异(21.3对17.6个月; HR = 0.84,95%CI,0.69-1.02,P = .0840)。
研究者评估了这些共同主要终点:中位随访时间为12.9个月。
最新消息,阿特珠单抗(Atezolizumab)目前在国内也已经提交申请,国内的乳腺癌患者有望在下半年就可以用到这个药物。
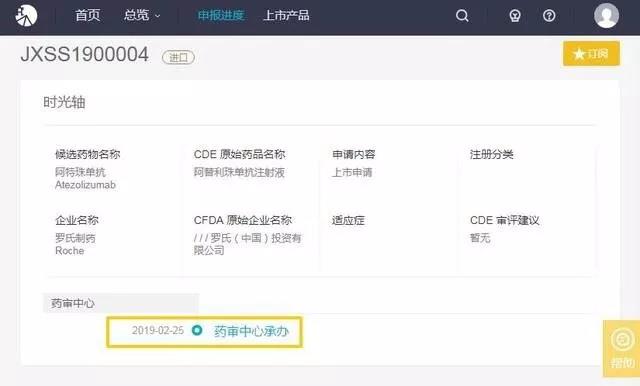
三阴性乳腺癌是一种极具侵袭性的疾病,治疗方案有限。受这一重大进展的鼓舞,期望将这一组合能够尽快在国内通过批准,带给三阴性乳腺癌患者。
虽然阿特珠单抗(Atezolizumab)在中国申请的首个适应症是肺癌,但对乳腺癌的患友也有好消息,国内该药正在进行相关临床研究。详情请点击文章底部往期精彩回顾:
《评价PD-L1针对三阴型晚期乳腺癌患者的安全性和耐受性》
如果符合条件的乳腺癌患者有望免费获得治疗。
如果对于阿特珠单抗(Tecentriq)希望有更多了解,也可以通过登录易加医APP对接咨询美国或香港的肿瘤专科医师,获取专业的第二诊疗意见。
易加医将持续关注该药物的上市进展,在第一时间将国内上市价格,相关慈善政策作及时发布。敬请关注!
易加医 2019.3.9



 浙公网安备 33010602004553号
浙公网安备 33010602004553号


