入选标准
1. 年龄 18 岁至 70 周岁的, 复发的经病理学或组织学证实的不可切除的或者晚期恶性实体瘤受试者, 如下:,
- 卵巢癌;增加:1-3线治疗的铂耐药的卵巢癌患者;铂耐药的定义:患者最后一次接受含铂类药物的时间到复发的时间小于等于6个月。(线数的计算:1.新辅助和/或辅助治疗算一线;2.维持治疗不算一线,连同之前的治疗算做一线)
- 三阴乳腺癌(ADC暴露后)、 子宫内膜癌、
- 肺鳞癌
- 黑色素瘤
- 滑膜肉瘤等肉瘤
- 食管鳞癌(一线后全身治疗);
- 小细胞肺癌,末线患者;
- 其他实体瘤(宫颈癌和胰腺癌不收)
- 结直肠癌和胰腺癌两个癌种(只要KRAS G12V)
2. 签署知情同意书
3.经研究者判断无可适用的治疗方案,或无法耐受目前可用的治疗方案
4.受试者经 HLA 分型确认含有 HLA-A*11:01 亚型或者经 HLA 分型确认含有 HLA-A*02:01 亚型且肿瘤 PRAME 表达经 IHC 检测
阳性
5.KRAS-G12V 突变队列:肿瘤 KRAS G12V 突变阳性, (尽量使用2年内采集的石蜡包埋肿瘤样本或新鲜肿瘤样本)
6.依照 RECIST 1.1 标准, 至少有一个可以进行影像学测量评估的肿瘤病灶
7.ECOG 评分 0-1 分
8.在白细胞单采前和清淋前受试者预期生存期不低于 3 个月
9. 受试者单采前和清淋前器官功能良好,见表 4:
表 4:受试者器官功能良好的评定指标
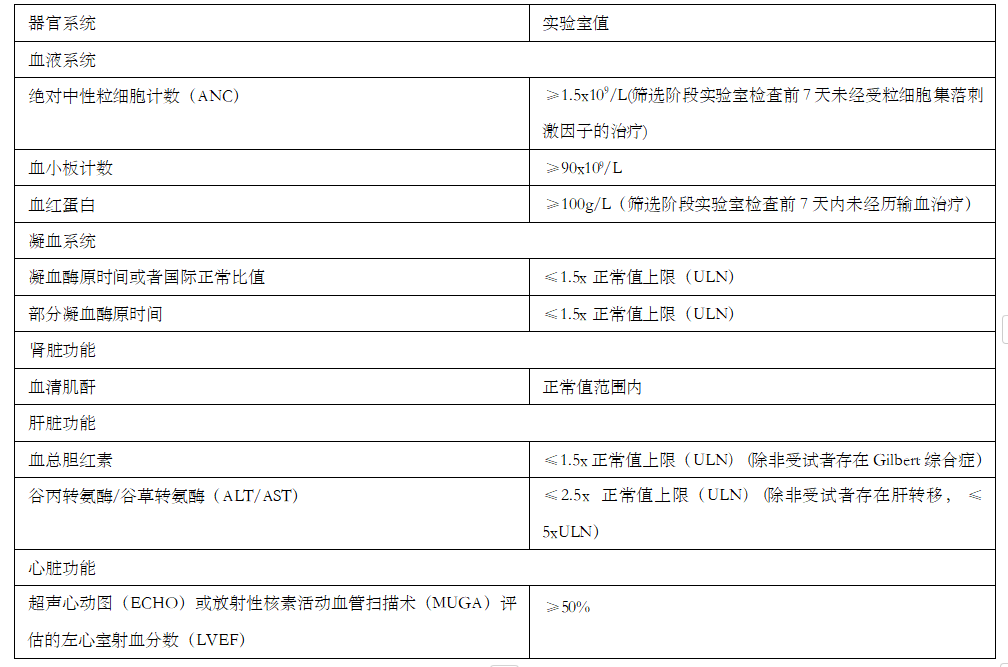
10. 肺功能:≤CTCAE1 级呼吸困难和在室内空气环境下 SaO2≥92%
11.血管通路足以进行白细胞单采
12. 具有潜在生育能力的女性(所有生理上能怀孕的妇女)必须在单采和清淋前通过血妊娠试验检测为阴性
13. 具有潜在生育能力的女性必须同意在签署入组主知情同意书开始使用有效避孕方法 1 年或者在血液中无法发现 NW-101 存在的 4 个月之后,以较长者为准。
排除标准
1.受试者接受过以下治疗:
• 单采前 2 周内和清淋前 1 周内接受过细胞毒性的化疗;
• 单采前 2 周内和清淋前 1 周内接受过抗体类治疗(包括但不限于:单抗治疗, 免疫检查点抑制剂治疗)或者其他生物治疗;
• 单采前 2 周内和清淋前 72 小时内接受过治疗剂量的皮质类固醇(定义为大于 20mg/d 的泼尼松或者同等药物)。但近期或者最近使用吸入性或口服用激素不作为排除标准, 其他的例外请见 5.5 章节;
• 单采前 2 周内和清淋前 1 周内接受过免疫抑制剂(例如: 钙调神经磷酸酶抑制剂、甲氨蝶呤或其他化疗药物,霉酚酸酯、雷帕霉素、沙利度胺、免疫抑制性抗体,如抗 TNF、抗 IL-6 或抗 IL-6 受体);
• 单采前 1 周内和清淋前 1 周内使用过小分子药物/酪氨酸激酶抑制剂和其他与骨髓抑制相关的抗癌治疗药物。注意:对于选择性的 EGFR 和 ALK/ROS-1 抑制剂并不需要洗脱期, 除非这些抑制剂是靶向 VEGFR、PDGFR 或者 c-Kit 受体的多酶抑制剂
• 单采前 4 周内和清淋前 4 周内使用过其他研究用药物;
• KRAS-G12V 突变队列中:单采前或清淋前使用过靶向 KRAS-G12V 突变的治疗
• KRAS-G12D 突变队列中: 单采前或清淋前使用过靶向 KRAS-G12D 突变的治疗
• 单采前 4 周内和清淋前 4 周内使用过其他研究用药物;
• 受试者在单采前 4 周内接受过大手术外科操作;根据研究者的评估, 受试者必须完全从手术相关的毒性中恢复 ·
• 任何基因治疗和或细胞治疗
• 单采前 4 周内和清淋前 1 周内使用过放疗作为抗肿瘤治疗
2. 在入组前,受试者因之前的抗肿瘤治疗而存在的毒性没有恢复到 1 级或者以下(除非是无临床意义的毒性,如:脱发, 白癜 风), 如果受试者存在一些被认为稳定的且不可逆转的 2 级毒性(例如:外周神经毒性)通过与新景智源的医学部人员沟通后是可以考虑入组的
3. 受试者如果对于环磷酰胺或者氟达拉滨以及其他在本研究使用药物的化学或者生物组成成分具有过敏反应史
4. 受试者具有需要使用激素或其他免疫抑制剂治疗的慢性/复发性(入组前 1 年内) 严重自身免疫疾病或活动性免疫疾病史
5. 受试者有症状性 CNS 转移
6. 柔脑膜病变或者癌性脑膜炎
7. 受试者在单采前 1 年内存在需要医学干预(免疫调节剂或者免疫抑制剂或者手术) 的慢性炎性肠病或者克罗恩病
8. 除了受试者原发肿瘤,受试者在单采前 3 年内有其他活动性恶性肿瘤史。除外: 经过充分治疗而不再需要治疗的恶性肿瘤(例
如:完全切除的非黑色素瘤皮肤癌或者完全治疗的原位癌,受试者必须从之前的肿瘤治疗中获得完全缓解才能入组本研究)
9. 受试者在筛选阶段存在具有临床意义的心电图异常或者平均 QTc 间期≥470 毫秒
10. 受试者存在以下未受控制的疾病:
• 进行中或者活动性的感染;
• 具有临床意义的心脏疾病(纽约心脏病学会定义的>I 类的充血性心力衰竭; 入组前 6 个月内存在未控制的有临床意义的心律不齐; 急性冠脉综合征(入组前 6 个月内存在心绞痛或心肌梗死); 先天性长 QT 综合症既往史或家族史);
• 存在中枢神经出血和中风史, 或者入组前 6 个月内存在短暂性脑缺血或者可逆性缺血性神经障碍;
• 受试者存在间质性肺病
11. 受试者存在活动性 HIV 、HBV、HCV、新型冠状病毒或梅毒的感染, 定义如下:
• HIV 血清学阳性;活动性乙型肝炎感染;受试者如果乙肝表面抗原为阴性但是核心抗体为阳性, 必须乙肝 DNA 的拷贝数低于 当地医疗机构检测下限才可以入组,否则不能入组 ;活动性丙型肝炎感染(由丙肝 RNA 来决定) ;如果受试者的 HCV 抗体为阳性,则将通过 RT-PCR 进行 HCV RNA 的检查;新型冠状病毒感染、梅毒感染 ;CMV DNA 阳性
12. 正在进行哺乳或者已经怀孕的受试者
13. 受试者经过研究者判断很难遵从本研究的各种流程要求



 浙公网安备 33010602004553号
浙公网安备 33010602004553号


