关于 KRAS G12C 基因突变
RAS基因家族是第一个被发现的人类肿瘤基因,与人类肿瘤相关的主要有三种亚型:H-RAS、K-RAS和N-RAS。各种亚型的突变的频率和分布并不统一,其中KRAS最易突变,对人类癌症影响最大,约占RAS突变的85%。
大约有30%的癌症患者都存在KRAS突变,其中包括90%的胰腺癌,50%的结肠癌和25%的肺癌。KRAS突变是中国非小细胞肺癌(NSCLC)患者第二大常见的基因突变,占20~30%。
KRAS G12C突变占所有KRAS突变的44%,其中非小细胞肺癌中最常见,约占14%,其次大肠腺癌占3%~4%,胰腺癌占2%,全球每年超过100000人确诊为KRAS G12C突变。
KRAS也一直是最难攻克的癌症靶点之一,一度被认为不可成药。现在虽然有了Sotorasib和Adagrasib两种KRAS靶向药,但疗效只能说是差强人意。但国内尚无相关药物上市。
在非小细胞肺癌(NSCLC)中,Sotorasib和Adagrasib的客观缓解率(ORR)都只有40%左右,结直肠癌中的ORR更是分别只有9.7%和19%。
目前国产的KRAS G12C靶向也成“井喷”式发展,并且取得了非常亮眼的数据。
小编也为大家盘点了KRAS G12C 相关靶向药的临床研究最新数据药
1.加科思 JAB-21822(格来雷塞)与JAB-3312联合用药
此次公布的是格来雷塞(JAB-21822)与JAB-3312联合用药的I/IIa期研究,该试验共设7个剂量组,包括400毫克与800毫克格来雷塞与不同剂量及给药间歇的JAB-3312联用,旨在通过不同剂量组探索安全性、有效性及耐受性,为后续用于上市的注册临床试验提供依据。
截至2023年8月4日,共144例KRAS G12C突变患者入组,其中包括129位非小细胞肺癌患者,14位结直肠癌患者,及一位胰腺癌患者。
在129位非小细胞肺癌患者中,107位患者经历过至少一次RECIST 1.1标准的肿瘤评估,其中有58位为一线治疗的患者(包括7个剂量组),ORR为65.5%(38/58),DCR为100%。其中在800毫克格来雷塞及2毫克JAB-3312联用的剂量组中[1],ORR为86.7%(13/15)。由于患者还在治疗中,中位无进展生存期(mPFS)和持续缓解时间还在观察中。
在所有剂量组中,三级和四级TRAE(治疗相关不良事件)的发生率为39.6%,而800毫克格来雷塞及2毫克JAB-3312联用的剂量组中[1],三级和四级TRAE的发生率为36.7%。
2.益方生物D-1553(Garsorasib)
在今年的ESMO年会上,益方生物以壁报展示的形式(编号1622P)公布了Garsorasib(D-1553)在KRAS G12C突变的晚期胰腺癌(PCa)患者中的早期临床研究数据。结果显示,Garsorasib单药治疗在KRAS G12C突变的PCa患者中展现出良好的耐受性和临床活性,确认的客观缓解率(ORR)为35.7%(5/14),疾病控制率(DCR)为85.7%(12/14),中位无进展生存期为8.54个月(95%CI, 2.73, NA)。
Garsorasib(D-1553)联合西妥昔单抗(Cetuximab)在KRAS G12C突变结直肠癌(CRC)患者中的一项II期研究结果成功入选本次大会,由中山大学肿瘤防治中心徐瑞华教授进行口头报告。
数据显示:Garsorasib联合西妥昔单抗在既往经治的KRAS G12C突变结直肠癌患者中客观缓解率(ORR)达45%,中位无进展生存期(mPFS)为7.6个月。
国家药品监督管理局(NMPA)已于2023年12月18日正式受理益方生物D-1553片的上市申请,并于2024年1月被纳入优先审评审批:用于既往经一线系统治疗后疾病进展或不可耐受的、并且经检测确认存在 KRAS G12C 突变的局部晚期或转移性非小细胞肺癌的治疗,有望冲刺国内首款KRAS G12C抑制剂上市产品。
3.默沙东 MK-1084
在剂量探索临床试验中,MK-1084作为单药治疗实体瘤患者达到22%的ORR(包含所有剂量)。MK-1084与pembrolizumab联用,治疗NSCLC时达到71%的ORR,在PD-L1高表达(TPS≥50%)患者中的ORR达到75%。
4.恒瑞医药 HRS-4642
HRS-4642的早期临床试验结果。在18名携带KRAS G12D突变的实体瘤(主要为NSCLC)患者中,1名NSCLC患者获得部分缓解,11名患者疾病稳定。
5.安进 sotorasib(索托拉西布)
安进公司公布了KRAS G12C抑制剂sotorasib与EGFR靶向单抗panitumumab联用,治疗携带KRAS G12C突变的转移性结直肠癌患者的3期临床试验结果,这些患者对化疗耐药。试验结果显示,在中位随访时间为7.8个月时,sotorasib(960 mg)组合的中位无进展生存期(PFS)为5.6个月,sotorasib(240 mg)组合的PFS为3.6个月,研究者选择的化疗组PFS为2.2个月。
6.Mirati Therapeutics MRTX849(adagrasib 阿达格拉西布)
adagrasib与PD-1抑制剂pembrolizumab联用,一线治疗携带KRAS G12C突变的非小细胞肺癌(NSCLC)患者的2期临床试验结果。在PD-L1高表达(TPS≥50%)的患者中,确认客观缓解率(ORR)为63%。中位随访时间为10.1个月时中位PFS尚未达到。
下面是我们正在招募的KRAS 位点突变相关临床研究
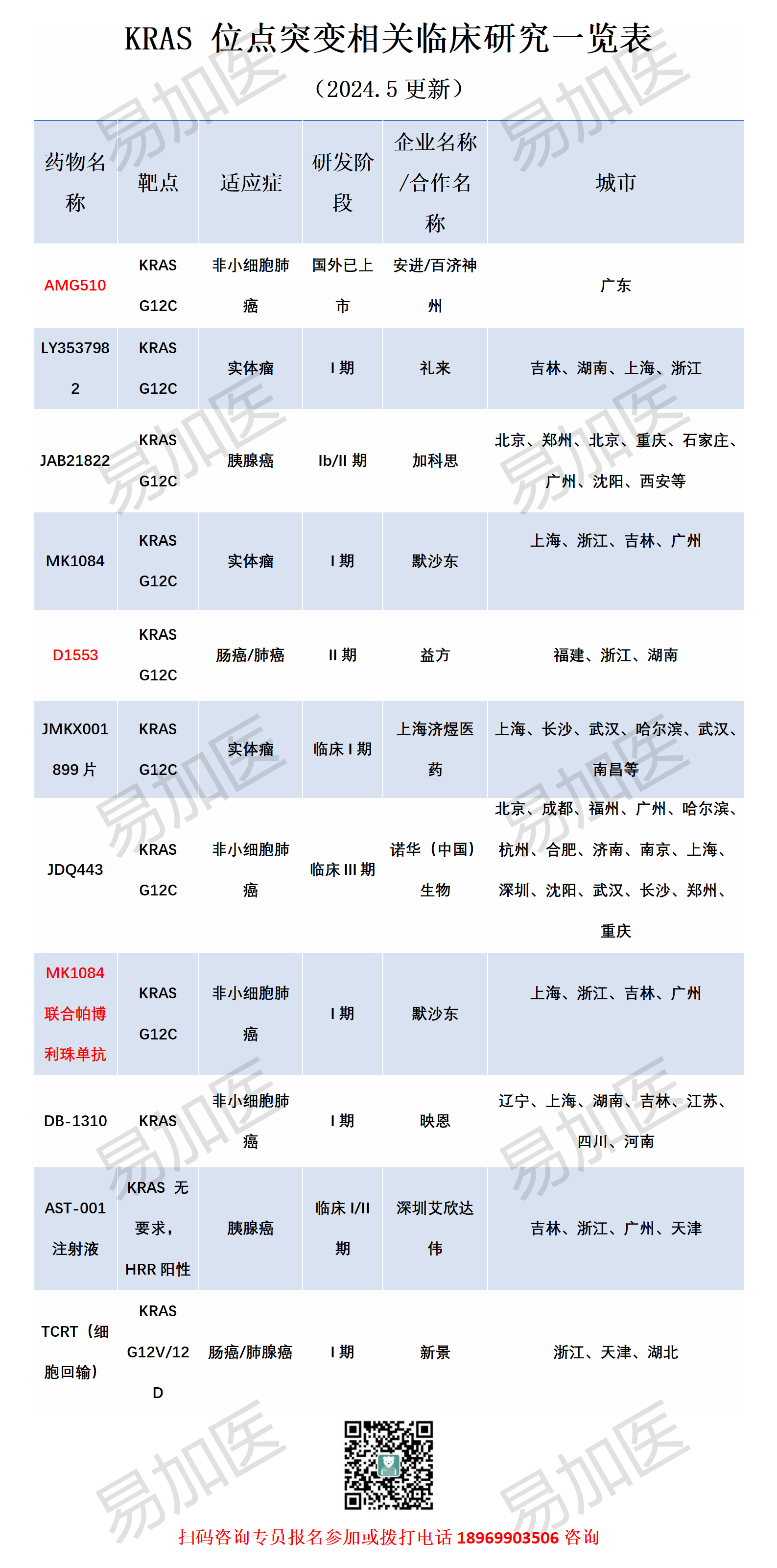
目前已有多位患者通过我们参加了KRAS G12C的临床,最好的治疗效果已经超过一年,目前在组里用药治疗
患者受益:
⭐可抢先获得国际前沿新药使用机会,对晚期肿瘤患者来说可能是新的生机(一个新型抗癌药物的研发,从临床前实验到批准进行临床试验,再到上市一般需要7~10年的时间,这对于一名晚期癌症患者来说,在不参与临床试验的情况下,很难有机会等到药物上市的日子);
⭐入组后相关的检查、治疗、用药均为免费,并有相关补贴,大大减轻家庭经济负担!
⭐大型三甲医院一线专家团队为你的治疗保驾护航!
如果您有意参加,请点击链接申请,招募专员会详细为您介绍本研究概况及您需要配合事项,并初步判断您是否符合入选要求,即使您不愿意参加本研究,也不会受到任何对您不利的影响,并对您的相关信息进行保密。
注:做了基因检测的病友可以拿出报告看看,一旦存在突变,可以扫描下方二维码添加专员看看是否有机会接受国内新药治疗,看不懂的病友也可以添加专员解读报告。



 浙公网安备 33010602004553号
浙公网安备 33010602004553号


